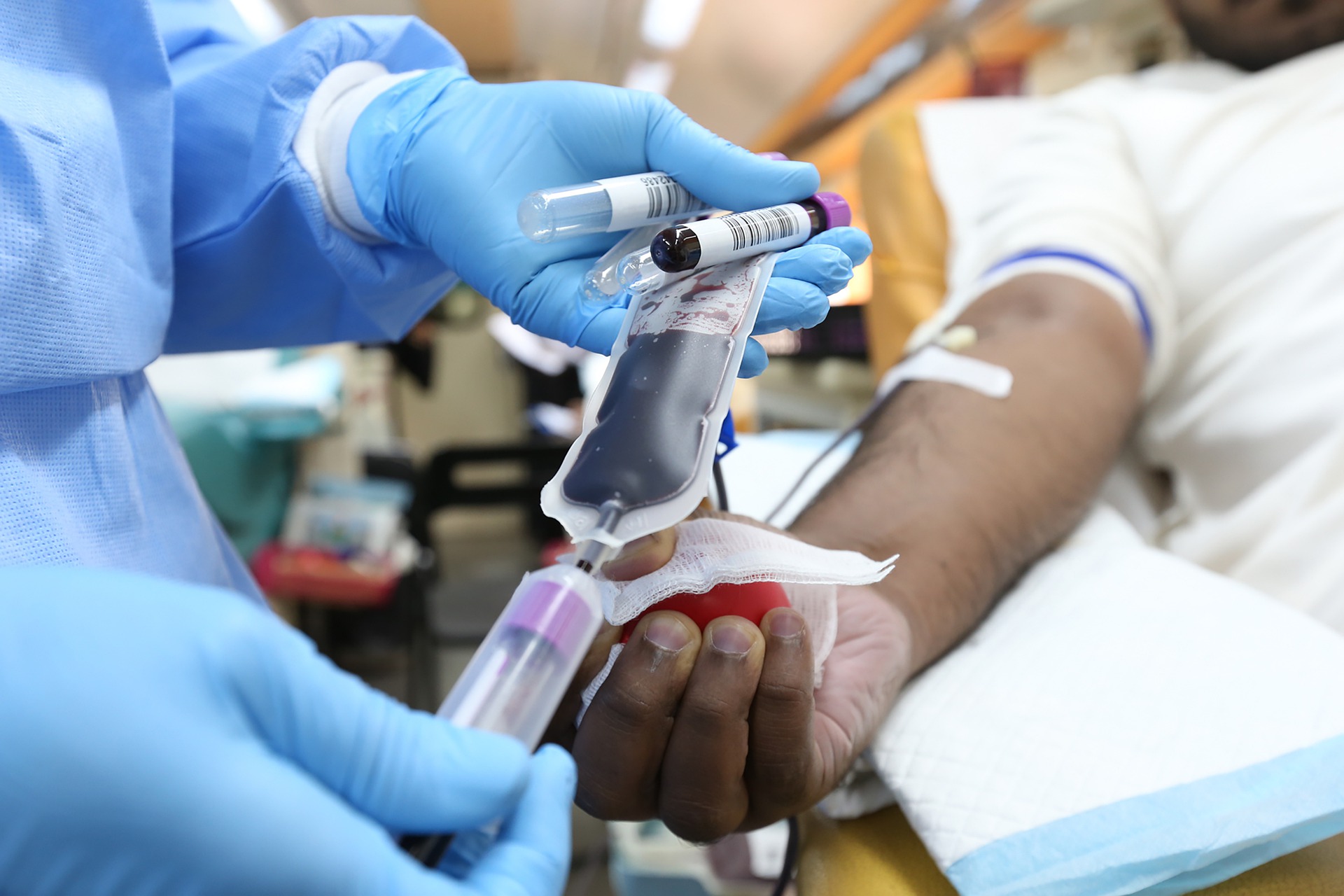
Le plasma riche en plaquettes (PRP), également appelé gel plaquettaire autologue, le plasma riche en facteurs de croissance (PRGF), le concentré plaquettaire (PC), est essentiellement une concentration accrue de plaquettes autologues en suspension dans une petite quantité de plasma après centrifugation. Fondamentalement, le sang du patient est prélevé et centrifugé à des vitesses variables jusqu’à ce qu’il se sépare en trois couches : le plasma pauvre en plaquettes (PPP), le PRP et les globules rouges. On utilise généralement deux centrifugations.
La première (« Hard spin ») sépare le plasma pauvre en plaquettes (PPP) de la fraction rouge et du plasma riche en plaquettes (PRP). La seconde (« Soft spin ») sépare la fraction rouge du PRP.
Le matériau ayant la densité la plus élevée (PRP) sera déposé au fond du tube. Immédiatement avant l’application, un activateur/agoniste plaquettaire (thrombine bovine topique et 10 % de chlorure de calcium) est ajouté pour activer la cascade de coagulation, produisant un gel plaquettaire. L’ensemble du processus dure environ 12 minutes et produit une concentration de plaquettes de 3 à 5 fois supérieure à celle du plasma natif.
Les plaquettes jouent un rôle fondamental dans l’hémostase et sont une source naturelle de facteurs de croissance.
Les facteurs de croissance, stockés dans les granules de plaquettes α-, comprennent le facteur de croissance dérivé des plaquettes (PDGF), le facteur de croissance analogue à l’insuline (IGF), le facteur de croissance de l’endothélium vasculaire (VEGF), le facteur angiogénique dérivé des plaquettes (PDAF) et le facteur de croissance transformant bêta (TGF-β). La libération de ces facteurs de croissance est déclenchée par l’activation des plaquettes qui peut être déclenchée par une variété de substances ou de stimuli tels que la thrombine, le chlorure de calcium ou le collagène.
Les facteurs de croissance sont impliqués dans les étapes clés de la cicatrisation des plaies et des processus de régénération, notamment la chimiotaxie, la prolifération, la différenciation et l’angiogenèse. Selon la définition de la PRP, on peut supposer que ces facteurs de croissance sont présents à des concentrations accrues dans la PRP. En plus des facteurs de croissance (GF), les plaquettes libèrent de nombreuses autres substances (par exemple, la fibronectine, la vitronectine, le sphingosine 1-phosphate, etc…) qui sont importantes pour la cicatrisation des plaies. Un avantage de la PRP par rapport à l’utilisation d’un seul facteur de croissance humain recombinant est la libération de multiples facteurs de croissance et de différenciation lors de l’activation des plaquettes. Récemment, la configuration morphologique et moléculaire de la PRP a été signalée, elle a montré que la PRP est une structure de fibrine par rapport aux plaquettes qui a le potentiel de soutenir une matrice régénérative.
L’utilisation de la PRP dans l’augmentation douce et dure a pour but d’accélérer la vascularisation du greffon.
D’améliorer la cicatrisation des tissus mous, de réduire la morbidité postopératoire et d’améliorer la régénération osseuse. Parmi les avantages de l’utilisation d’une PRP autologue, citons l’absence de risque de réactivité croisée, de réaction immunitaire ou de transmission de maladie.8 En outre, l’utilisation de la PRP améliore la manipulation des matériaux de greffe particulaires et facilite le conditionnement dans un site de greffe, ce qui facilite le maintien de l’espace et la régénération osseuse potentielle.
Étant donné que le PRP contient plusieurs GF (par exemple, PDGF, VEGF, etc…) qui sont capables de stimuler l’angiogenèse et d’augmenter la différenciation des fibroblastes, il a été proposé d’utiliser le PRP pour favoriser la cicatrisation des tissus mous.2 Les recherches ont montré que le PRP et les produits analogues améliorent l’adhésion des greffons et minimisent les micro-mouvements, offrant ainsi l’environnement le plus avantageux pour l’acceptation des greffons.11,12 Il a également été proposé que le PRP accélère la maturité et l’épithélialisation des plaies, d’où une diminution de la formation de cicatrices. Le PDGF et le facteur de croissance épidermique (EGF) sont les principaux facteurs de croissance impliqués dans la migration des fibroblastes, la prolifération et la synthèse du collagène. Des concentrations accrues de ces facteurs de croissance sont probablement à l’origine de l’accélération de la cicatrisation des tissus mous, qui serait au moins 2 à 3 fois plus rapide que la normale.
Pour les tissus durs, les facteurs de croissance libérés par la PRP sont susceptibles d’affecter les cellules vitales locales telles que les ostéoblastes.
L’ajout de PRP aux cellules stromales a démontré des propriétés angiogéniques et ostéogéniques dans des modèles animaux. L’utilisation de PRP pour améliorer la régénération osseuse a été documentée dans des défauts parodontaux, des cavités d’extraction, lors de la mise en place d’implants, et dans des procédures de régénération osseuse guidée autour des implants, y compris l’augmentation des sinus.
L’un des principaux inconvénients de l’augmentation osseuse est le temps de guérison prolongé qu’elle nécessite. L’un des principaux inconvénients de l’augmentation osseuse est le temps de guérison prolongé qu’elle nécessite. Par conséquent, l’une des principales raisons proposées pour l’utilisation de la PRP est un temps de guérison réduit. Une accélération de la régénération osseuse a également été démontrée dans les défauts parodontaux distaux des deuxièmes molaires lorsque la PRP est ajoutée au moment de l’extraction des troisièmes molaires touchées. Malheureusement, ces résultats ne peuvent pas être utilisés pour expliquer les effets bénéfiques de la PRP, car les biopsies n’ont été prélevées sur aucun des sites de contrôle.
Dans les études animales, lorsque l’os spongieux de la crête iliaque a été utilisé comme matériau de greffe pour les sinus liftés avec ou sans PRP, les biopsies ont montré que la PRP et les sites témoins étaient tous deux des facteurs de risque. Voir https://fr.wikipedia.org/wiki/Plasma_riche_en_plaquettes pour en savoir plus